Os inflamáveis (gasolina e o etanol), possuem comportamentos específicos no meio ambiente.
Todas as vezes que vamos abastecer nossos veículos precisamos ter a consciência desses comportamentos dos inflamáveis.
Aqui, abro um parênteses para explicar o porquê denominamos gasolina e etanol como inflamáveis e não como combustíveis.
Popularmente denominamos combustíveis essas duas substâncias por relacionarmos o produto com o veículo automotivo (carro, moto, ônibus, caminhão etc.), porém, saibamos que normativamente essas substâncias (gasolina e etanol), não são classificadas como combustíveis, mas sim como inflamáveis.
A Norma Regulamentadora – NR 20 Segurança e Saúde no Trabalho com Inflamáveis e Combustíveis, na seção 20,3 determina:
20.3.1 –. Líquidos inflamáveis: são líquidos que possuem ponto de fulgor ≤ 60º C.
20.3.1.1 – Líquidos que possuem ponto de fulgor superior a 60ºC (sessenta graus Celsius), quando armazenados e transferidos aquecidos a temperaturas iguais ou superiores ao seu ponto de fulgor, se equiparam aos líquidos inflamáveis.
20.3.2 – Gases inflamáveis: gases que inflamam com o ar a 20ºC e a uma pressão padrão de 101,3 kPa ou 1,03 bar ou 14,69 PSI ou 0,99975327 atm.
20.3.3 – Líquidos combustíveis: são líquidos com ponto de fulgor > 60º C e ≤ 93º C.
A gasolina possuiu seu ponto de fulgor – PF = – 38°C, já o etanol possuiu ponto de fulgor – PF = 17°C, portanto, classificados como líquidos inflamáveis de acordo com a subseção 20.3.1 da NR 20.
A gasolina e o etanol, assim como todas as substâncias químicas possuem em suas propriedades físico-químicas, as seguintes características:
- Densidade absoluta e relativa;
- Volume no ambiente;
- Taxa de evaporação;
Esses são alguns fatores importante para serem estudados nesse artigo.
O fator mais importante para o comportamento da gasolina e do etanol é a temperatura ambiente, pois, é ela, quem irá conduzir esse comportamento diretamente nas propriedades físico-químicas das substâncias.
A seguir apresentaremos as propriedades físico-química das duas substâncias de interesse para este estudo:
GASOLINA:
Fórmula química: C8H18;
Massa Molar: 114,00 g/mol;
Ponto de Fulgor – PF: -38°C;
Limite Inferior de Inflamabilidade – LII: 1,3% v/v;
Limite Superior de Inflamabilidade – LSI:7,1% v/v;
ETANOL:
Fórmula química: C2H6O;
Massa Molar: 46,07 g/mol;
Ponto de Fulgor – PF: 12,8°C;
Limite Inferior de Inflamabilidade – LII: 3,3% v/v;
Limite Superior de Inflamabilidade – LSI:19,0% v/v;
O primeiro estudo a ser apresentado é o da densidade absoluta das duas substâncias.
DENSIDADE ABSOLUTA
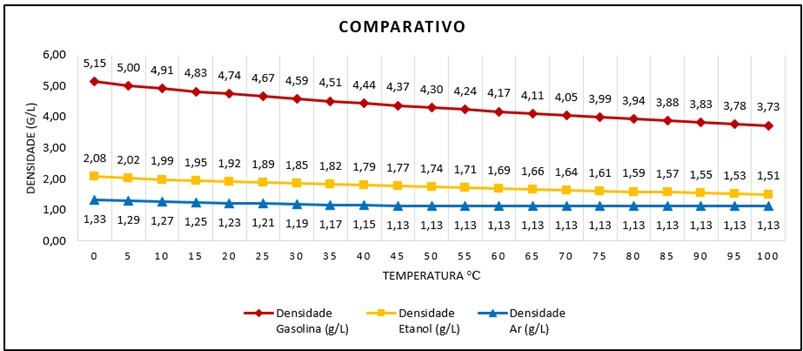
As temperaturas para o estudo foram de 0°C até 100°C.
A gasolina apresentou densidade absoluta maior em relação ao etanol e o ar atmosférico.
O etanol apresentou densidade absoluta maior em relação ao ar atmosférico e menor em relação a gasolina.
O ar atmosférico apresento densidade absoluta menor em relação a gasolina e o etanol.
Para o estudo considerou-se cálculos para a densidade absoluta do ar atmosférico até a temperatura de 45°C = 1,13 g/l, sendo que a partir de 50°C se manteve a mesma densidade de 45°C.
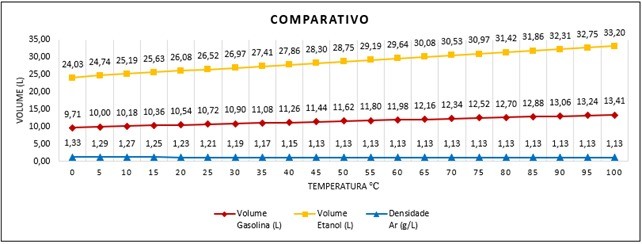
VOLUME NO ESPAÇO (AMBIENTE)
Para o estudo de volume no espaço (ambiente), iremos considerar quantidades muito pequenas de produtos 50 ml para ambos os inflamáveis.
O gráfico mostra que se pegarmos 50 ml de produto e transformarmos em vapor, o volume ocupado no espaço (ambiente), a uma temperatura de 0°C = 24,03L (gasolina), 9,71L (etanol) e a 100°C = 33,20L (gasolina), 13,41 (etanol).
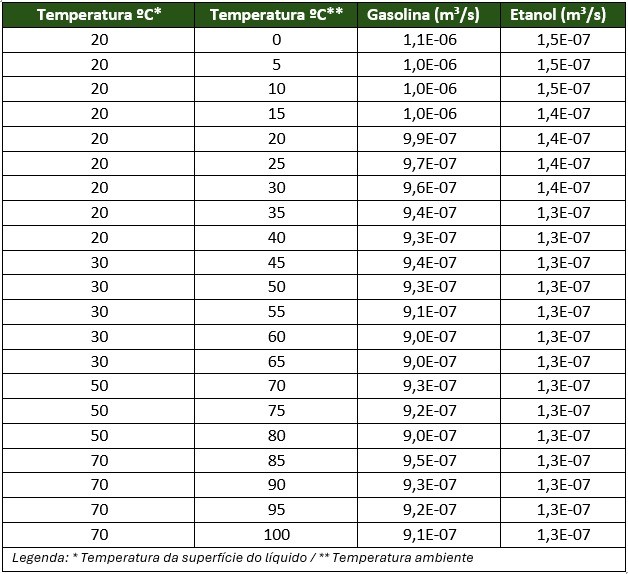
TAXA DE EVAPORAÇÃO
A taxa de evaporação é a quantidade de produto (gasolina e etanol) que evapora constantemente em função da temperatura ambiente, temperatura da superfície do líquido e a área em que o produto está ocupando.
Para este estudo foi considerado as temperaturas da tabela abaixo e uma área fixa de 0,28m² para os dois produtos.
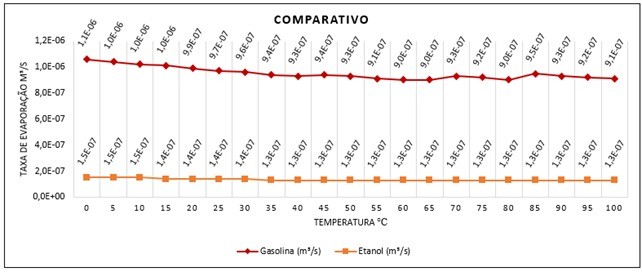
A taxa de evaporação da gasolina é maior que a do etanol, portanto, maior volume dentro do espaço (ambiente).
INFLAMABILIDADE
A inflamabilidade é a quantidade de produto necessário para formar uma atmosfera explosiva em 1m³ de volume.
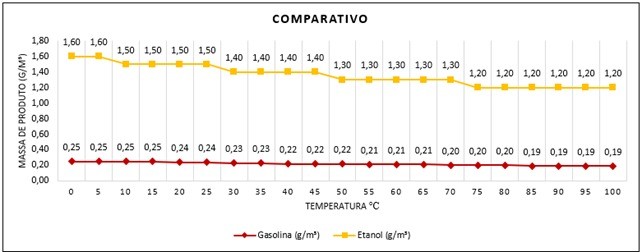
A gasolina precisa de uma quantidade menor em gramas para uma atmosfera explosiva em 1m³ que o etanol.
CONCLUSÃO:
De acordo com o vídeo é possível verificar que o motivo do princípio de incêndio no abastecimento pode ter sido pelos seguintes fatores:
- A Temperatura ambiente poderia estar elevada;
- A temperatura da moto poderia estar elevada, aumentando assim a o volume de vapor internamente, a taxa de evaporação e consequentemente a quantidade em massa para uma atmosfera explosiva.
- O tanque possuiu uma área em m² pequena, aumentando a agitação do inflamável no compartimento.
- A velocidade de abastecimento da bomba poderia ter influência junto com a temperatura externa e interna, pois, quanto maior a velocidade do produto dentro do tanque, maior sua agitação, maior o volume, a taxa de evaporação e a massa para inflamabilidade.
RECOMENDAÇÕES:
- Abasteça sempre no início do dia e/ou a noite quanto a temperatura ambiente estiver menor;
- Abasteça nos primeiros momento em que sair com o veículo;
- Solicite ao frentista que use a menor velocidade no abastecimento (link do vídeo abaixo).





